
往期回顾:
个体化细胞治疗技术国家地方联合工程实验室多年来深入研究分析GMP(药品生产质量管理规范)和GAMP5(良好自动化生产实践指南),结合自身丰富的细胞领域实验室成果,转化为细胞行业信息化解决方案,为研发、生产、临床端提供既满足业务需求,又符合法律法规的信息化软件,打造细胞全生命周期闭环管理,填补了国内生物医药行业细胞治疗产品的信息化短板。平台软件已在全国多家医院、综合细胞库、细胞公司、CRO公司等落地使用,极大提升了客户的工作效率,获得了客户认可。
实验室归纳总结了自身的细胞行业应用软件开发经验,从对GMP标准规范、GAMP5方法指南的解读,规范及指南如何运用到细胞行业应用软件的设计中,以及实验室依此打造出的细胞全生命周期管理平台各类行业应用软件介绍,分四大章节讲述。
参考文件:
NMPA 2010版 《药品生产质量管理规范》
NMPA 《GMP附录-细胞治疗产品》(征求意见稿)
NMPA 《GMP附录-计算机化系统》
ISPE 《GAMP5》
FDA 《21 CFR Part 11》(《联邦法规21章》第11款)
本章节介绍实验室结合细胞行业特点,GMP规范要求,GAMP5方法指南,创造的细胞全生命周期管理平台理念,以及研发落地的各类细胞行业应用软件。
个体化细胞治疗技术国家地方联合工程实验室,多年来一直深入研究分析GMP(药品生产质量管理规范)和GAMP5(良好自动化生产实践指南),结合自身丰富的细胞领域实验室成果,打造出了细胞全生命周期管理平台(CELLALL)。从技术上保证用户统一,接口统一,数据集中,在平台框架内,开发出各类应用承载研发、生产、临床三大环节的不同业务场景。
通过使用软件系统集中积累研发、生产、临床过程数据,采用细胞唯一编码串联,贯穿细胞全生命周期,从而做到实时监管,反向溯源。
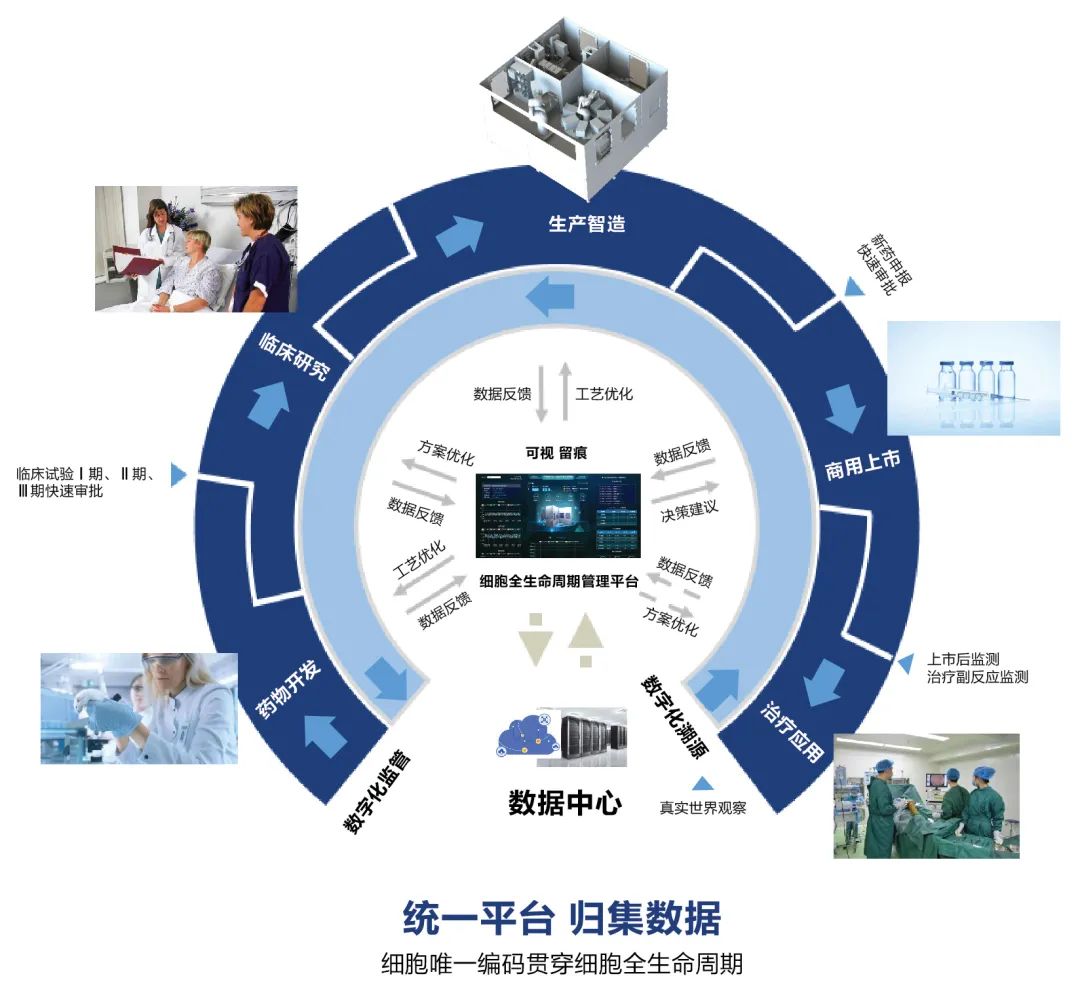
平台制备管理模块包括SOP执行引擎,生产任务调度,生产监控大屏,配液管理,质量管理,偏差管理,检测管理,样本库管理,资源管理等功能。为细胞制备工程师,制备主管,QC,QA,生产管理者,公司管理层等角色提供不同服务。
制备记录同上期所述,包括符合GMP规范的批生产记录和检验记录,通过系统生成制备档案和检测档案,供QA检查放行。
● 核心思想
依据GMP追溯核心要求:来源可溯(供体),中间可控(生产),去向可追(临床应用)。
● 平台追溯模型设计
1) 追溯数据模型
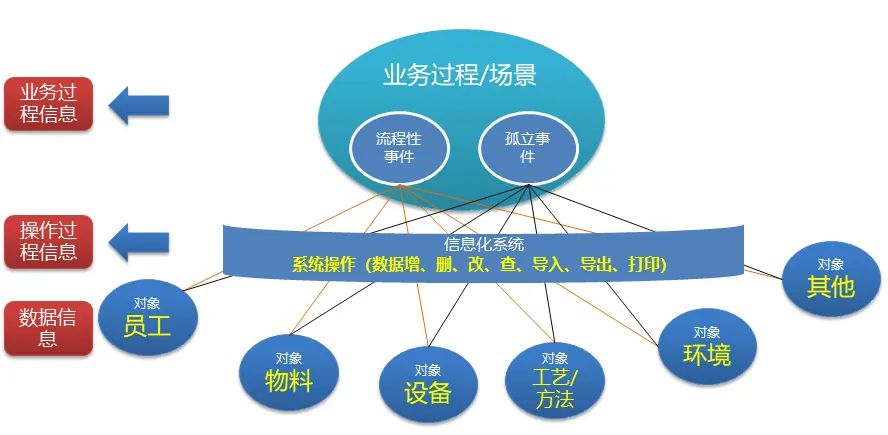
平台设计了“过程-事件-对象”的关联追溯数据模型,基于此模型系统做了如下记录:
一、业务过程记录(存储方式:业务日志)
在业务过程/场景记录过程中各事件节点的人机料法环信息,用于业务追溯。例如细胞制备这个业务过程,包括离心/添加缓冲液/移液枪吸取/培养基留样/细胞检测等流程性事件或动作,每个事件都记录对应的时间,即时环境,操作人员,物料,工艺方法等信息。
二、系统操作记录(存储方式:操作日志)
详尽记录信息系统所有操作信息,用于系统底层问题排查。
2) 业务追溯关键字
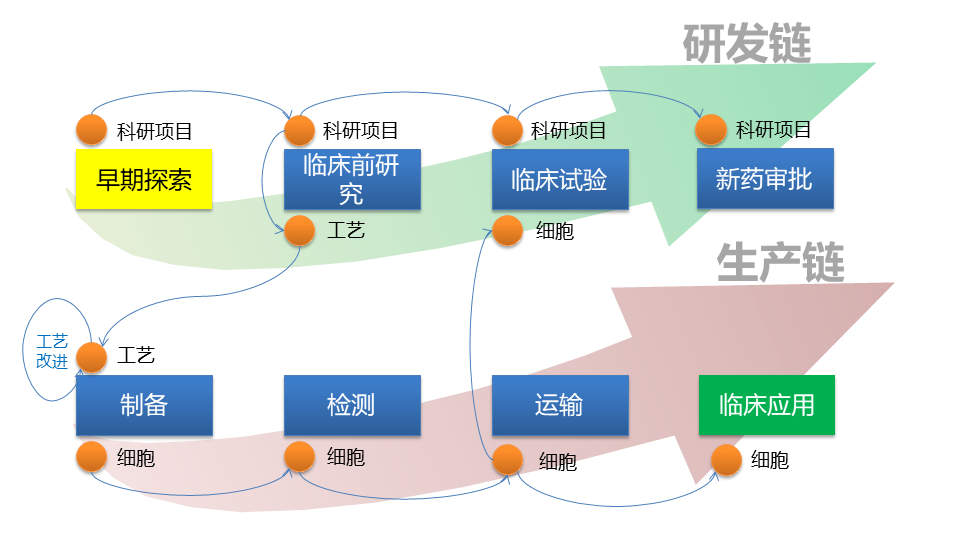
平台中的细胞全生命周期数据,采用如下key值关联:研发端(工艺ID)-生产端(工艺ID,细胞ID)-临床端(细胞ID),用以实现研发-生产-临床应用全流程追溯,能从临床应用环节溯源到生产环节和科研环节,而不是传统意义的、单一的生产环节追溯。在细胞生产环节发现偏差,或者在细胞临床应用环节发生医疗事故,不光能反向从生产环节找原因,还能根据生产所使用的工艺,从科研环节找原因,最终实现真正意义的细胞全生命周期追溯。
平台对细胞终产品赋予细胞唯一编码,用于生产、运输、临床应用环节的追溯。生产过程中的半成品编码,参考ISBT128编码标准制定,内含批次号关联,并包括位置,供体ID,阶段等过程信息,为来源可溯(供体),中间可控(生产),去向可追(临床应用)提供唯一主线。
目前平台开发了面向终端用户的“细胞质量查询系统”,让终端用户能够随时随地查询到自己储存的、使用的细胞质量,做到用户放心、安心;
还有面向细胞公司、监管机构的“细胞追溯系统”,让细胞公司管理人员能够实时溯源质量问题,为监管机构提供实时监管,实时审批的数字化服务。
我们是如何按照GAMP的指导方法进行开发的?
我们按照GAMP的指导方法,首先制定了相关管理程序,严格按照管理程序进行开发,开发过程中的技术文档,都按要求输出。
我们制定的管理程序部分如图:
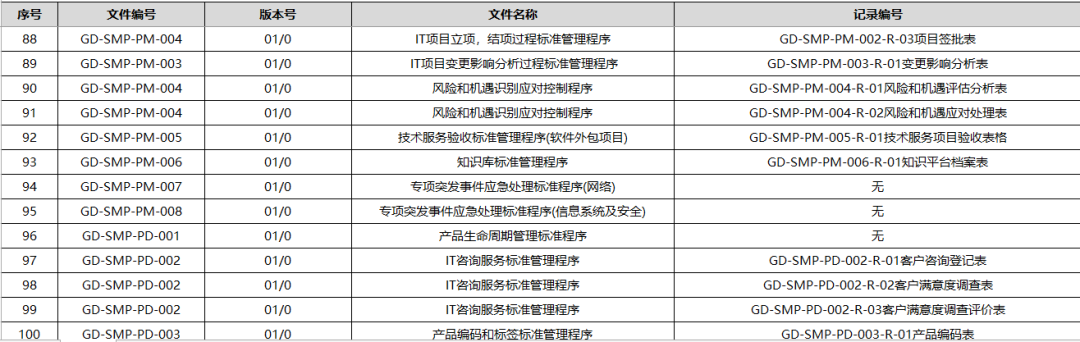
下图为我们某项目计划输出的技术文档:
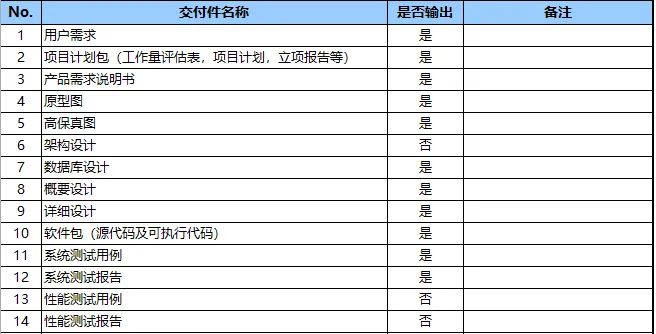
经过多年的法律法规研读以及行业实战开发积累,我们逐步整理输出了细胞追溯体系架构,编码要求,追溯基本数据集等平台技术规范。
细胞信息化追溯体系架构如图:
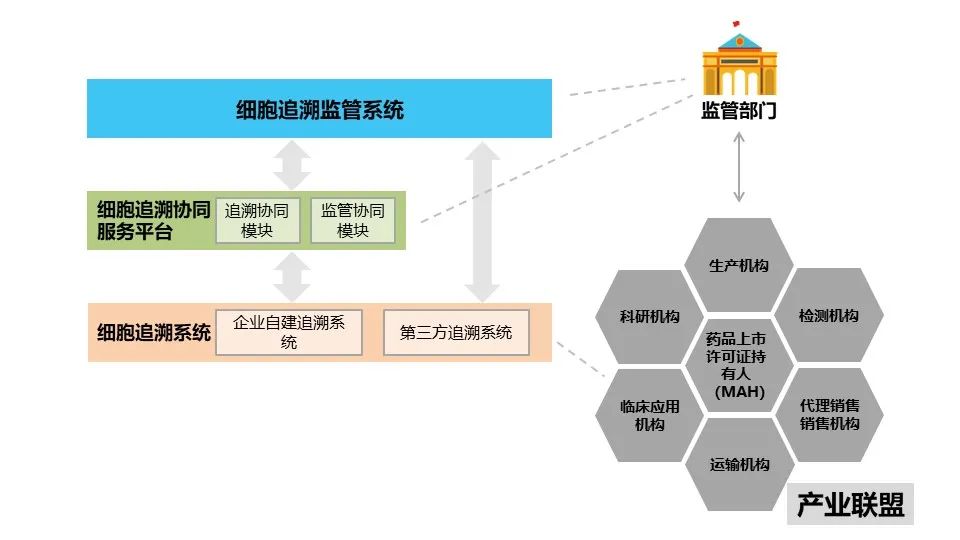
其中,
《细胞追溯基本数据集》――规定了与细胞信息化追溯体系建设相关的细胞追溯基本数据集分类、数据集与细胞追溯数据产生方关系及数据集内容。细胞追溯基本数据集可分为基础信息数据子集,应用信息数据子集和应用操作过程记录三类。适用于规范追溯数据产生方采集和存储满足相关要求的追溯数据。
《细胞追溯数据交换基本技术要求》――规定了细胞信息化追溯体系中细胞追溯数据交换的方式、数据格式、数据内容和安全要求。适用于规范细胞追溯系统、细胞追溯协同服务平台、细胞追溯监管系统等数据交换方之间进行细胞追溯数据的交换。
《细胞追溯编码要求》――规定了细胞追溯码的术语和定义、编码原则、编码对象、基本要求、构成要求、载体基本要求、发码机构基本要求以及药品上市许可持有人、生产机构基本要求。适用于临床试验研究机构、制备机构、检测机构、药品代理销售机构、运输机构、临床应用机构和发码机构等追溯参与方,针对在全球范围内销售和使用的细胞选择或使用符合本标准的细胞追溯码。
《临床治疗,保健指标数据集》――规定了细胞治疗和保健的一般检查、实验室检查、医技检查、专科量表及检查指标。收集全量指标数据,分析重点指标的发展趋势,指标间的关联关系,用以评判临床疗效。
下面,我们将介绍细胞全生命周期管理平台(CELLALL)核心应用系统。
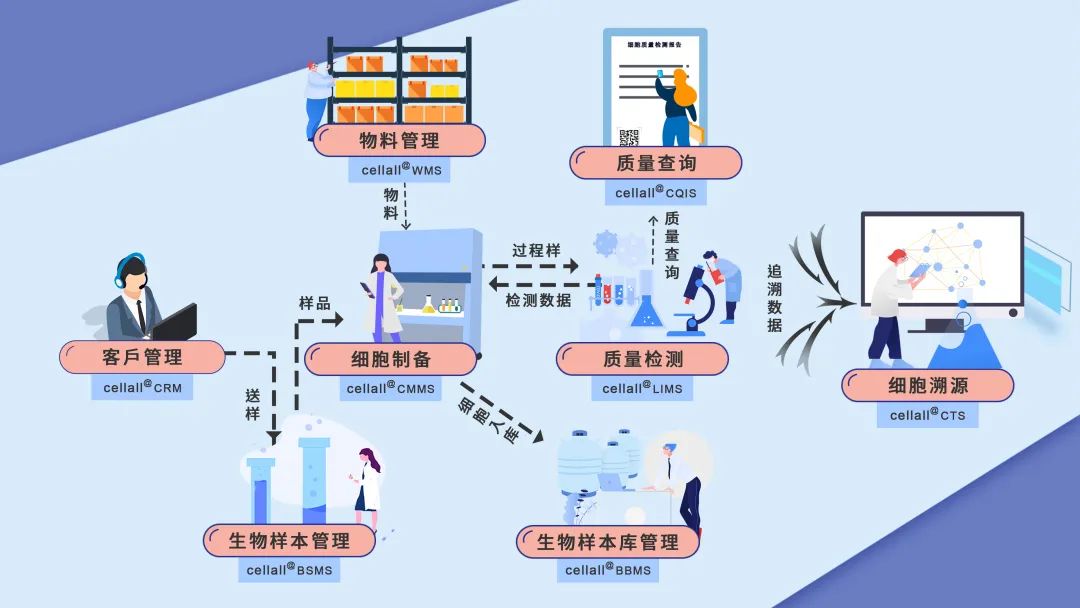
图1:生产信息化体系图
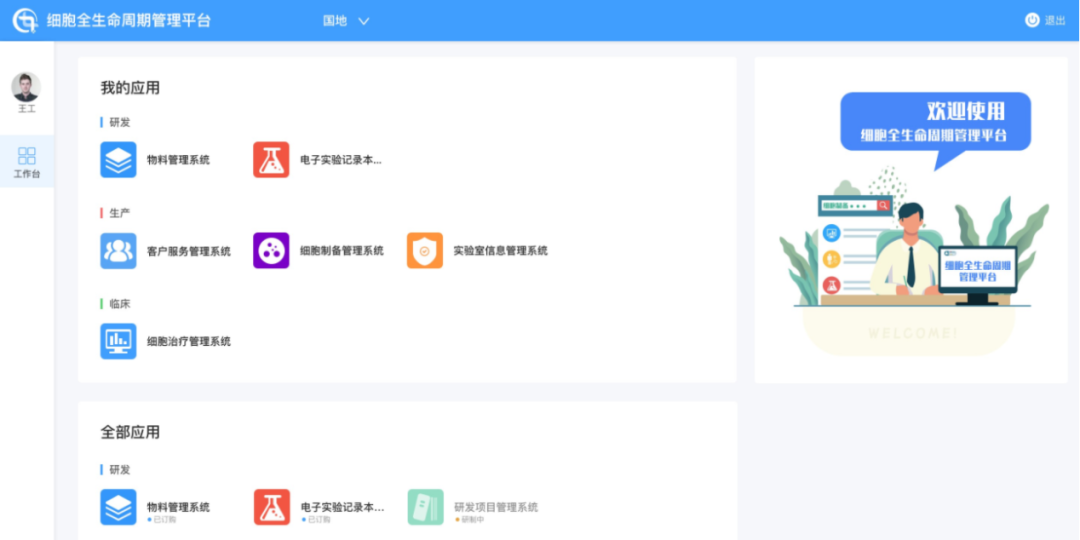
图2:细胞全生命周期管理平台首页
面向生物医药实验室研发人员,解决研发过程重复记录及低效记录,无法有效跟踪追溯问题,实验数据合规化记录和注册数据整合问题,提供实验记录、复核、追溯及报告管理等功能。
系统支持多中心科研项目的实验记录协作和数据共享。具有完善的数据保护和保存机制,协助研发部门完成从项目实验纸质记录注册申报到电子化记录申报的转型。
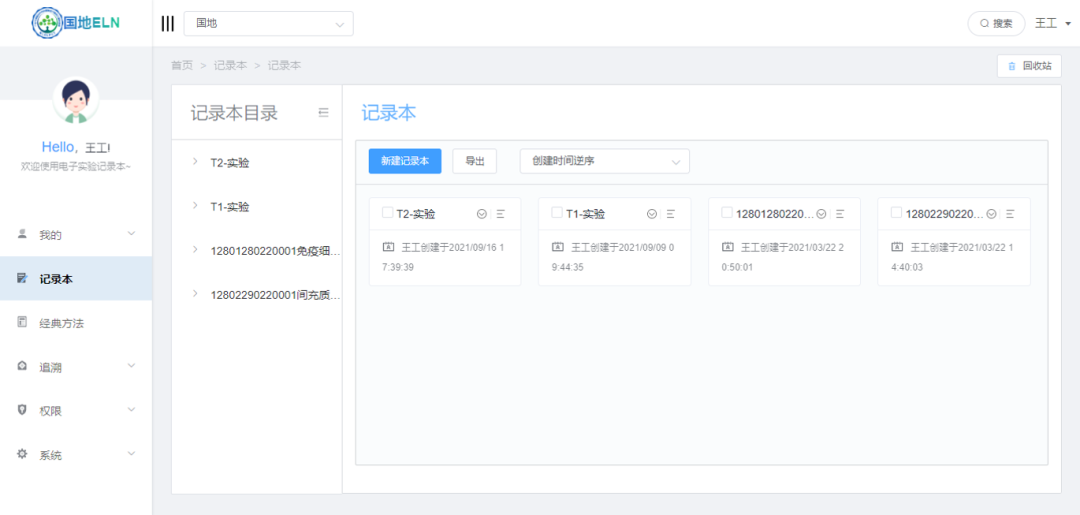
图3:系统操作界面
生物医药领域专用物料管理系统,可用于科研及生产制造场景,支持试剂、耗材入库、出库、盘点、物料溯源等业务,报表功能覆盖库存、出入库、呆滞料及需求预测等,另具备低库存预警、近效期预警等特性,与电子实验记录系统及细胞制备系统可无缝对接。
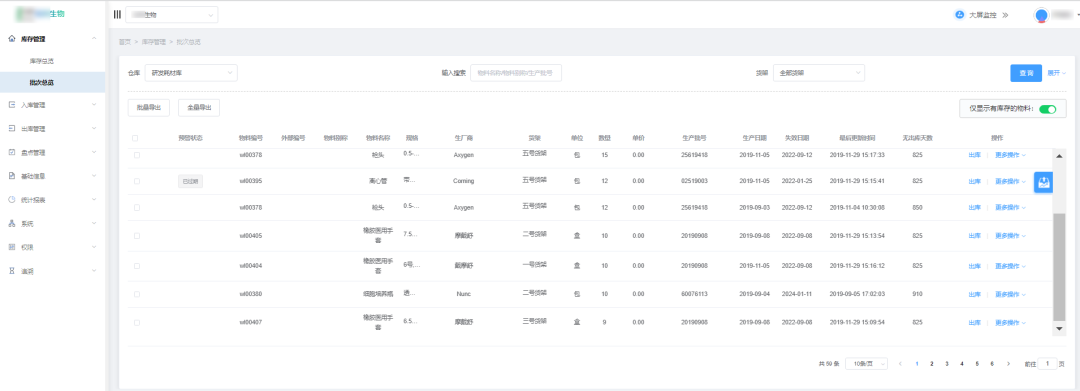
图4:系统操作界面

图5:物料监控大屏
基于合规要求和全面的细胞质量控制策略,协助细胞生产企业完成从传统制备管理迁移到无纸化的,全流程的细胞制备生产管理。同时解决生产过程成本控制、效率管理等问题。系统支持干细胞及免疫细胞的制备管理,包括制备计划,制备任务,过程记录,过程跟踪,质量管理,效率分析,业务报表等。
涵盖细胞生产全过程质量因素管理,细胞储存管理,可视化、合规、全程可溯,适应远程交互审计。
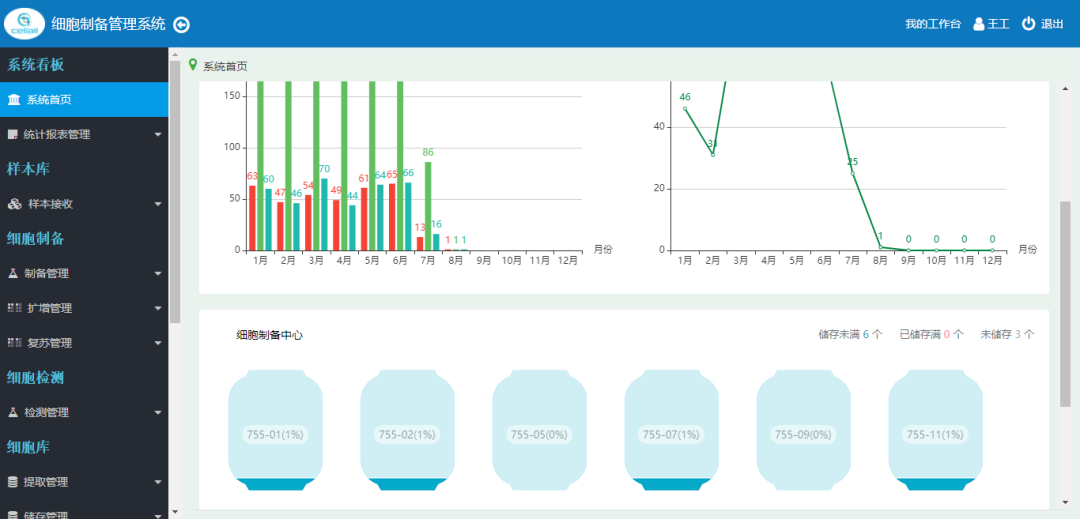
图6:系统操作界面

图7:生产监控大屏
针对检验实验室的整体环境而设计,是一个包括了信号采集设备、数据通讯软件、数据库管理软件在内的集成系统。实现检验实验室数据和信息的收集、分析、报告和管理,协助完善检验实验室的人、机、料、法、环质量因素的管理,从而提高检验实验室的工作效率以及质量控制水平。
高度集成检验仪器,提供便捷自助服务,智能化检验,灵活报告管理,全程可预警、可追溯。
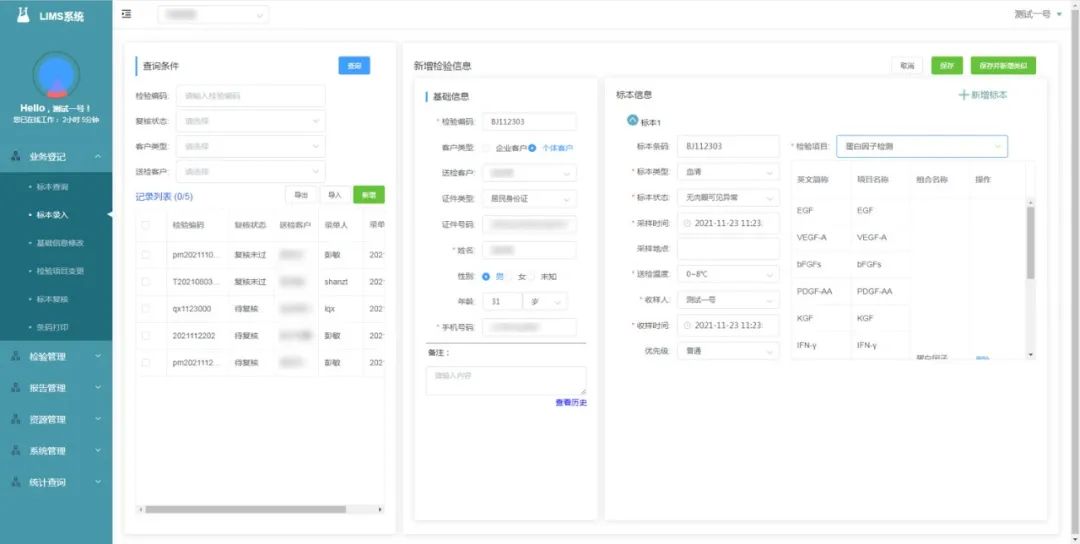
图8:系统操作界面
整合研发端,生产端,临床端数据,一物一码全程可视,契合法规,支持双向追溯,多方位追溯,支持远程交互式实时监管。
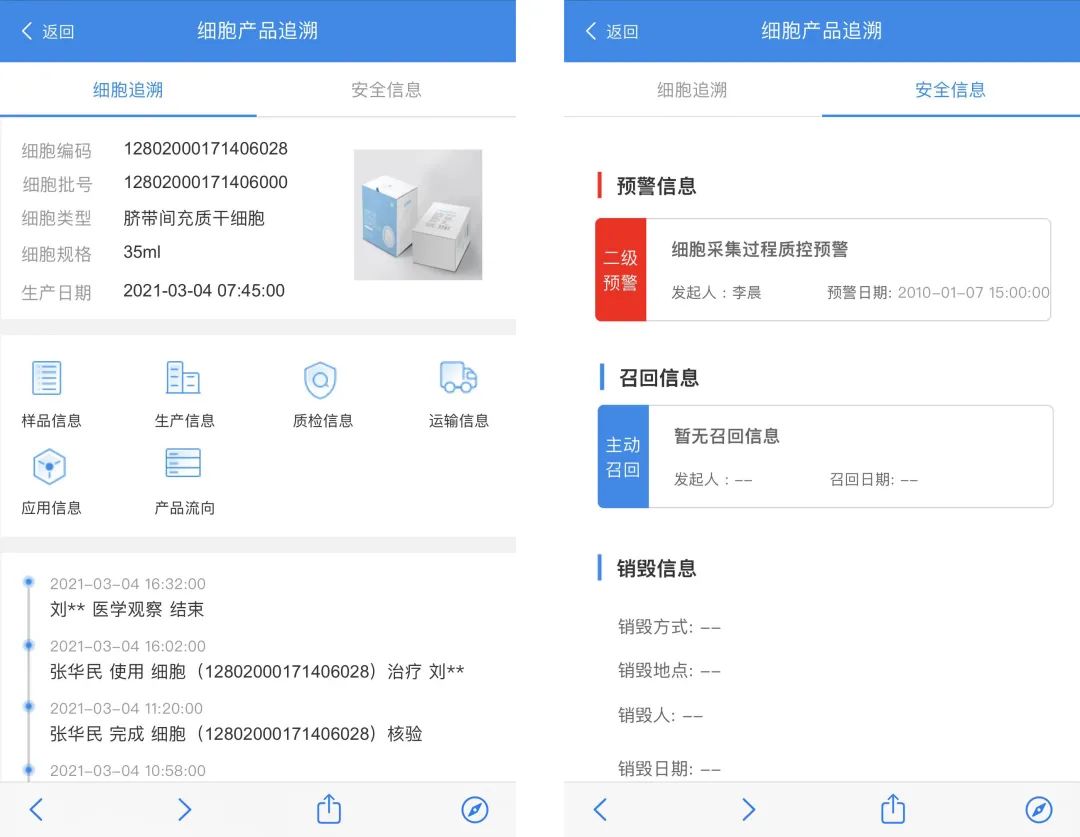
图9:系统操作界面
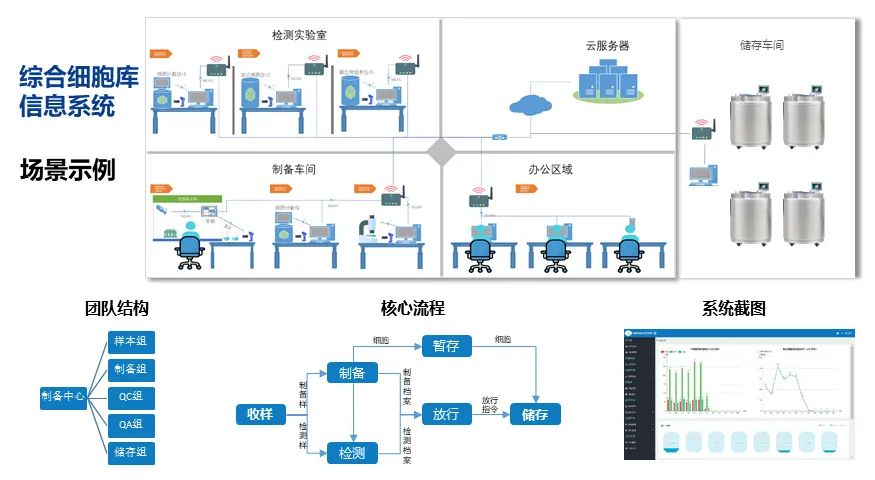
图10:综合细胞库信息系统场景示例图
细胞全生命周期管理平台的物料管理、制备管理、质量管理等模块,搭载配套至全自动细胞智造系统,实现软硬件融合,智能智造一体化。为生物医药领域的GMP生产过程的合规与监管赋予全生命周期智能化和数字化能力。

图11:深圳细胞智造中心实景图
目前细胞行业,甚至整个生物医药行业,迫切需要信息化革命,以辅助企业顺利开展合法合规的,质量可控的生产。但革命的道路是曲折而又艰难的,如何通过信息化手段支撑传统企业平稳过渡,是一个非常复杂的课题。可能会在信息化实施的很长一段时间内,在企业生产效率和用户满意度上会形成风暴,但终会天开云散,风和日丽。
